Mastiplan LC inj.
Léčba klinických mastitid u krav v laktaci vyvolaných Staphylococcus aureus, koaguláza negativními stafylokoky, Streptococcus agalactiae, Streptococcus dysgalactiae, Streptococcus uberis a Escherichia coli citlivými na cefapirin.
1. NÁZEV VETERINÁRNÍHO LÉČIVÉHO PŘÍPRAVKU
Mastiplan LC, 300 mg/20 mg (Cefapirinum/Prednisolonum), intramamární suspenze pro laktující krávy
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jeden 10ml aplikátor obsahující 8 g olejovité suspenze obsahuje:
Léčivá látka:
Cefapirinum (ut Cefapirinum natricum) 300 mg
Prednisolonum 20 mg
Pomocné látky:
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Intramamární suspenze
Popis: bělavá/žlutá až růžová, olejovitá, homogenní suspenze
4. KLINICKÉ ÚDAJE
4.1 Cílové druhy zvířat
Krávy v laktaci
4.2 Indikace supřesněním pro cílový druh zvířat
Léčba klinických mastitid u krav vlaktaci vyvolaných Staphylococcus aureus, koaguláza negativními stafylokoky, Streptococcus agalactiae, Streptococcus dysgalactiae, Streptococcus uberis a Escherichia coli citlivými na cefapirin.
4.3 Kontraindikace
Nepoužívat u zvířat alergických na cefalosporinová antibiotika nebo jiná b-laktamová antibiotika nebo jiné složky přípravku.
4.4 Zvláštní upozornění pro každý cílový druh
Žádné.
4.5 Zvláštní opatření pro použití
Zvláštní opatření pro použití u zvířat
Nepoužívejte čistící ubrousky na struky sotevřenými ranami.
Přípravek by se měl používat na základě vyšetření citlivosti a vsouladu sprincipy oficiální a národní antibiotické politiky.
Aplikátor lze použít pouze jednorázově pro jeden struk.
Zvláštní opatření určené osobám, které podávají veterinární léčivý přípravek zvířatům
Peniciliny a cefalosporiny mohou po injekci, inhalaci, požití nebo kožním kontaktu vyvolat hypersenzitivitu (alergii). Hypersenzitivita na peniciliny může vést ke zkřížené citlivosti na cefalosporiny a naopak. Alergické reakce na tyto látky mohou být ojediněle vážné.
Nemanipulujte spřípravkem, pokud víte, že jste hypersenzitivní na peniciliny nebo cefalosporiny nebo pokud Vám bylo doporučeno nepracovat stakovými přípravky.
Zacházejte spřípravkem se zvýšenou opatrností a dodržujte všechna doporučená opatření, abyste předešli expozici.
Pokud se Vám po expozici objeví příznaky, například kožní vyrážka, vyhledejte pomoc lékaře a ukažte mu toto varování. Otok obličeje, rtů a očí nebo potíže při dýchání jsou mnohem závažnějšími příznaky a vyžadují urgentní lékařskou pomoc.
Po použití čistících ubrousků si umyjte ruce a používejte ochranné rukavice, pokud se očekává nebo je podezření na podráždění kůže isopropylalkoholem.
4.6 Nežádoucí účinky (frekvence a závažnost)
Nejsou známy.
4.7 Použití v průběhu březosti, laktace nebo snášky
Mastiplan LC je určen k použití během laktace.
Laboratorní studie u myší, potkanů, králíků a křečků nepodaly důkaz o teratogenním, fetotoxickém účinku a maternální toxicitě.
Nejsou dostupné žádné informace indikující reprodukční toxicitu (včetně teratogenity) u skotu.
Během březosti a u chovných zvířat používat pouze po zvážení terapeutického prospěchu a rizika příslušným veterinárním lékařem, protože nebyly provedeny žádné zvláštní studie u cílových druhů zvířat.
4.8 Interakce s dalšími léčivými přípravky a další formy interakce
Nejsou známy.
4.9 Podávané množství a způsob podání
Obsah jednoho aplikátoru se aplikuje bezprostředně po dojení do každé postižené čtvrtě mléčné žlázy přes strukový kanálek ve 12-hodinových intervalech po čtyři následující dojení.
Každý aplikátor obsahuje 300 mg cefapirinu a 20 mg prednisolonu.
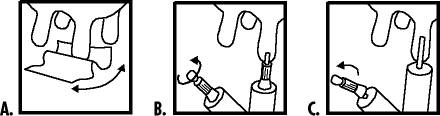
Před aplikací se postižená čtvrť mléčné žlázy úplně vydojí, struk se důkladně očistí a vydezinfikuje přiloženým čistícím ubrouskem. Je třeba zabránit kontaminaci aplikační trysky aplikátoru. Ulomte vršek krytky a jemně zasuňte asi 5 mm (B) nebo odstraňte celou krytku a jemně zasuňte celou délku aplikační trysky aplikátoru (C) do strukového kanálku. Aplikujte celý obsah jednoho aplikátoru do čtvrtě. Přípravek rozptylte jemnou masáží struku a mléčné žlázy postižené krávy.
4.10 Předávkování (symptomy, první pomoc, antidota), pokud je to nutné
Neuplatňuje se.
4.11 Ochranné lhůty
Maso: 4 dny (96 hodin)
Mléko: 5,5 dne (132 hodin)
5. FARMAKOLOGICKÉ VLASTNOSTI
ATCvet kód: QJ51RV01
Farmakoterapeutická skupina: spojení antibakteriálních látek a kortikosteroidů.
5.1 Farmakodynamické vlastnosti
Cefapirin je cefalosporin první generace, který inhibuje syntézu buněčné stěny. Je baktericidní sčasově závislým mechanismem účinku a vyznačuje se širokým terapeutickým spektrem účinku.
In vitro byla prokázána účinnost proti běžným grampozitivním i gramnegativním zárodkům včetně Escherichia coli, Klebsiella spp., Arcanobacterium pyogenes, Staphylococcus aureus, koaguláza negativní stafylokoky,Streptococcus dysgalactiae, Streptococcus agalactiae a Streptococcus uberis.
Bylo prokázáno, že následující zárodky: Arcanobacterium pyogenes,Staphylococcus aureus, koaguláza negativní stafylokoky, Streptococcus uberis, Streptococcus dysgalactiae, Streptococcus agalactiae,Escherichia coli, Klebsiella spp. a Mannheimia haemolytica izolované během terénních studií provedených ve Francii, Velké Británii, Německu, Nizozemsku, Maďarsku, Itálii a Španělsku vobdobí let 1984 až 2005 byly citlivé na cefapirin.
Přehled hodnot MIC50 a MIC90 běžných bakteriálních, mastitidních patogenů izolovaných během klinických studií provedených vletech 1984-2005 jsou uvedeny v následující tabulce:
| Izolované bakteriální druhy | N | MIC50(µg/ml) | MIC90(µg/ml) |
| Staphylococcus aureus | 244 | 0,128 | 0,25 |
| Koaguláza negativní stafylokoky | 78 | 0,128 | 0,25 |
| Streptococcus uberis | 184 | 0,063 | 0,5 |
| Streptococcus dysgalactiae | 96 | 0,063 | 0,128 |
| Streptococcus agalactiae | 58 | 0,25 | 0,25 |
| Escherichia coli | 299 | 8 | 16 |
Během období 1984-2005 nebyl pozorován žádný pokles citlivosti mastitidních baktérií na cefapirin.
Prednisolon uplatňuje protizánětlivé vlastnosti prostřednictvím inhibice časných a pozdních fází zánětu. Po intramamárním podání u postižených zvířat prednisolon redukuje otok a následnou velikost postižené čtvrtě a podporuje návrat knormální teplotě.
5.2 Farmakokinetické vlastnosti
Po intramamárním podání přípravku Mastiplan LC se cefapirin a prednisolon vylučují především vmléce při dojení.Vstřebávání cefapirinu i prednisolunu do krevního oběhu je rychlé a omezené. Nepatrné vstřebané množství cefapirinu i prednisolonu se vylučuje hlavně vmoči.
Přehled koncentrací cefapirinu a prednisolonu v mléce během léčby je v následující tabulce:
| Léčivá látka | Průměrné koncentrace léčivých látek v mléce při dojeních vztažených k první aplikaci | ||||
| 0 | 1 | 2 | 3 | 4 | |
| Cefapirin(µg/ml) | 0 | 27,0 ± 6,2 | 30,2 ± 7,9 | 40,0 ± 8,8 | 34,6 ± 6,5 |
| Prednisolon(ng/ml) | 0 | 182,0 ± 61,7 | 100,8 ± 51,0 | 283,7 ± 129,8 | 101,5 ± 38,8 |
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Glycerol-monostearát
Hlinitokřemičitan sodno-vápenatý
Podzemnicový olej
6.2 Inkompatibility
Nejsou známy.
6.3 Doba použitelnosti
Doba použitelnosti veterinárního léčivého přípravku v neporušeném obalu: 2 roky
6.4 Zvláštní opatření pro uchovávání
Uchovávejte při teplotě do 25°C.
Uchovávejte aplikátory uvnitř vnější kartónové krabice.
6.5 Druh obalu a velikost balení
Druh obalu:
10ml aplikátor zpolyetylenu skládající se ze tří částí:
- válec
- píst
- víčko
Aplikátory jsou vloženy do sáčku potaženého hliníkovou fólií.
Velikosti balení:
Krabička s 1 sáčkem se 4 aplikátory a s 4 čistícími ubrousky.
Krabička s 1 sáčkem s20 aplikátory a s 20 čistícími ubrousky.
Na trhu nemusí být všechny velikosti balení.
Čistící ubrousky:
Papírové čistící ubrousky navlhčené 70% v/v roztokem isopropylalkoholu (2,4 ml/ubrousek).
6.6Zvláštní opatření pro zneškodňování nepoužitého léčivého přípravku nebo odpadu, pokud je jich třeba
Všechen nepoužitý veterinární léčivý přípravek nebo odpad, který pochází z tohoto přípravku, musí být likvidován podle národních předpisů.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Intervet International B.V.
Wim de Körverstraat 35
NL-5831 AN Boxmeer
Nizozemsko
8. REGISTRAČNÍ ČÍSLO(A)
96/019/07-C
9. DATUM REGISTRACE/ PRODLOUŽENÍ REGISTRACE
30. 5. 2007
10. DATUM REVIZE TEXTU
Červen 2013
Zákaz prodeje, výdeje a/nebo použití
Neuplatňuje se.
